-
胺
 胺
胺
胺,是氨分子中的一个或多个氢原子被烃基取代后的产物。可以是看作氨分子中的H被烃基取代的衍生物。胺类广泛存在于生物界,具有极重要的生理活性和生物活性,如蛋白质、核酸、许多激素、抗生素和生物碱等都是胺的复杂衍生物,临床上使用的大多数药物也是胺或者胺的衍生物,因此掌握胺的性质和合成方法是研究这些复杂天然产物及更好地维护人类健康的基础。
目录
- 1 基本信息
2 研究简史
3 物质结构
4 理化性质
5 制备方法
6 应用领域
7 毒理危害
基本信息
中文名:胺
所属领域:化学
酸碱特征:碱性
外文名:Amines
定义:氨分子中的氢被烃基取代而生成
组成:由一个氮原子、两个氢原子组成
常见形式:氨基酸
化学式:RNH2;RNHR';RN(R')R''
合成:卤化物氨解,酰胺还原等
研究简史
胺(àn) 氨NH3分子中部分或全部氢原子被烃基取代后而成的有机化合物,胺类大都具有碱性,能与酸结合而成盐,是制作合成染料、药物等的原料。
命名
简单胺的命名,以胺作为官能团,叫某胺,先写与氮原子相连接的羟基的名称,再以胺字作词尾;二元胺和多元胺的伯胺,当其氨基连在开链羟基或直接连接在苯环上时,可以称为二胺或三胺。
比较复杂的胺,可以看作是烃的衍生物来命名。季铵化合物可以看作是铵的衍生物来命名。
季胺化合物可以看作是胺的衍生物来命名。
基础定义
胺 【名】 氨分子里的氢被烃基或其他非酸性有机基取代后衍生出的一类有机化合物〖amine〗 胺 (è )【动】 肉类腐烂变臭〖(ofmeat)putrefy〗。 《广韵》:“胺,肉败臭。”
物质结构
胺中氮原子的结构,很像氨分子中的氮原子,是以三个sp杂化轨道与氢或烃基相连接,组成一个棱锥体,留下一个sp3杂化轨道由孤电子对占据。如果一个胺有三个不同基团时,应有一对对映体(见对映现象):
胺结构
但由于翻转胺分子中的孤电子对所需要的活化能很低,未能分离出其对映体。
实验证明,胺和氨分子具有棱形锥形结构,氮原子为sp3杂化,键角约为109度。在胺分子中,三个sp3杂化轨道分别于氢原子的s轨道或碳原子的杂化轨道重叠形成三个6键,剩下一对孤对电子占据第四个sp3轨道,位于棱椎体的顶端。
苯胺也是棱锥形的结构,但H-N-H键角较大,为113.9度,N-N-H平面与苯环平面交叉的角度为38度。
若胺分子中氮原子上连有三个不同的基团,则具有手性,理论上应存在一对对映体。
由于两个对映体之间的能垒相当低,约为21KJ/mol,在室温下就可以迅速相互转化,实际上这样的对映体尚未被分割出来。
在季铵盐中,氮的四个sp3轨道全部用来成键,如果氮原子上连有四个不同的基团,则存在着对映异构体。例如:碘化甲基稀丙基苯基苄基胺拆分为右旋和左旋光学异构体。
制法
胺在自然界中分布很广,其中大多数是由氨基酸脱羧生成的,
硝基化合物还原制取胺
理化性质
甲胺:CH3NH2
性质:又称一甲胺,在常温下为无色有氨臭的气体、或液体。易燃烧,其蒸气能与空气形成爆炸性混合物,爆炸极限5%-21%(4.95%-20.75%)。相对密度0.662,熔点为-93.5℃,沸点为-6.3~-6.7℃,-19.7℃(53.3kPa),-32.4℃(26.7kPa),-43.7℃(13.3kPa),-73.8℃(1.33kPa),分解温度250℃,闪点(闭杯)0℃,自燃点430℃,蒸气压(25℃)202.65Pa,临界温度156.9℃,临界压力4.073kPa,折射率1.351。液化后发烟体,比氨具有更强的碱性。易溶于水、乙醇和乙醚。
乙胺:CH3CH2NH2
无色有强烈氨味的液体或气体;蒸汽压 53.32kPa/20℃;闪点:<-17.8℃;熔点 -80.9℃;沸点16.6℃;溶解性:溶于水、乙醇、乙醚等;密度:相对密度(水=1)0.70;相对密度(空气=1)1.56;稳定性:稳定;危险标记 4(易燃气体),14(有毒品);主要用途:用于染料合成及作萃取剂、乳化剂、医药原料、试剂等。
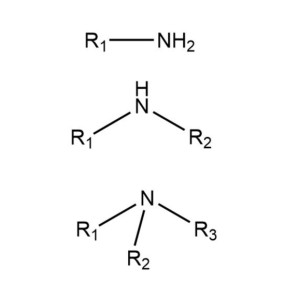
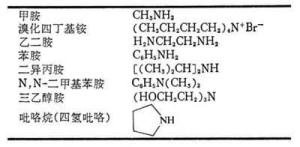
按照氢被取代的数目,依次分为一级胺(伯胺)RNH2、二级胺(仲胺)R2NH、三级胺(叔胺)R3N、四级铵盐(季铵盐)R4N+X-,例如甲胺CH3NH2、苯胺C6H5NH2、乙二胺H2NCH2CH2NH2、二异丙胺2NH、三乙醇胺(HOCH2CH2)3N、溴化四丁基铵(CH3CH2CH2CH2)4N+Br-。
根据胺分子中与氮原子相连的羟基种类的不同,胺可以分为脂肪胺和芳香胺。根据胺分子中与氮原子相连的羟基的数目,可以分为一级胺(伯胺,primary amine)、二级胺(仲胺,secondary amine)和三级胺(叔胺,tertiary amine)。如果胺分子中含有两个或两个以上的氨基(—NH2),则根据氨基数目的多少,可以分为二元胺、三元胺。
NH3(胺) RNH2(伯胺、一级胺) R2NH(仲胺、二级胺) R3N(叔胺、三级胺)
氢氧化胺或铵盐的四羟基取代物,称为季胺碱(quaternary ammonium hydroxide)或季铵盐(quaternary ammonium salt)。
NH4+铵 R4NOH季铵碱 R4NX季铵盐
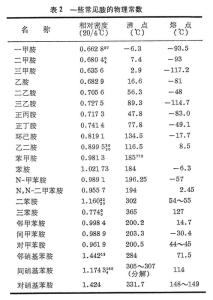
胺的物化性质
在常温下,低级脂肪胺是气体,丙胺以上是液体,高级脂肪胺是固体。低级胺有令人不愉快的,或是很难闻的气味。例如三甲胺有鱼腥味,丁二胺(腐胺)和戊二胺(尸胺)有动物尸体腐烂后的恶臭味。高级胺不易挥发,气味很小。芳胺为高沸点液体或低熔点固体,气味虽比脂肪胺小,但毒性比较大,无论是吸入他们的蒸气或皮肤与之接触都会引起中毒。有些芳胺,如β-萘胺,联苯胺还有致癌作用。
由于胺分子中的氮原子能与水形成氢键,所以低级脂肪胺在水中的溶解度都比较大。伯胺和仲胺能形成分子间的氢键,但由于氮原子的电负性小于氧原子,所以胺的氢键缔合能力比较弱,其沸点比相对分子质量相近的醇低。
胺与氨相似,分子中的氮原子上含有未共用的电子对,能与H+结合而显碱性。
R-NH2+HCl≒R-NH3+Cl-
胺的碱性以碱性电离常数Kb或其他负对数值pKb表示,Kb值越大或pKb值越小,胺的碱性越强。
制备方法
胺在自然界中分布很广,其中大多数是由氨基酸脱羧生成的。
胺
 胺的制备
胺的制备
合成
卤化物氨解(Ammonolysis of halides)
氨或胺氮上有孤对电子,作为亲核试剂与卤代烷发生亲核反应,按SN2机理进行。许多有机卤化物以氨水溶液或氨溶液处理则变成胺类:
X为卤素
RX + NH3 → RNH3 + X-
RNH3+X- → RNH2 + H2O + X-
用醇制备
胺的主要合成方法是氨的烷基化。工业上使用醇与氨合成有机胺:
ROH + NH3 → RNH2 + H2O
这些反应需要使用催化剂、特制仪器及额外纯化,因为得到的是一、二、三级胺的混合物,需要提高反应的选择性。
应用领域
胺的用途很广。最早发展起来的染料工业就是以苯胺为基础的。有些胺是维持生命活动所必需
胺
的,但也有些对生命十分有害,不少胺类化合物有致癌作用,尤其是芳香胺,如萘胺、联苯胺等。
 胺
胺
毒理危害
侵入途径:吸入、食入、经皮吸收。
健康危害:接触乙胺蒸气可产生眼部刺激、角膜损伤和上呼吸道刺激。液体溅入眼内,可致严重低度伤;污染皮肤可致灼伤。
一、应急处理处置方法
1、泄漏应急处理
迅速撤离泄漏污染区人员至上风处,并进行隔离,严格限制出入。切断火源。建议应急处理人员戴自给正压式呼吸器,穿消防防护服。尽可能切断泄漏源。若是气体,用工业覆盖层或吸附/吸收剂盖住泄漏点附近的下水道等地方,防止气体进入。合理通风,加速扩散。喷雾状水稀释、溶解。构筑围堤或挖坑收容产生的大量废水。如有可能,将残暴余气或是漏出气用排风机送至水洗塔或与塔相连的通风橱内。漏气容器要妥善处理,修复、检验后再用。若是液体,用砂土、蛭石或其它惰性材料吸收。若大量泄漏,构筑围堤或挖坑收容;用泡沫覆盖,降低蒸气灾害。用防爆泵转移至槽车或专用收集器内,回收或运至废物处理场所处置。储罐区最好设稀酸喷洒设施。
废弃物处置方法:用控制焚烧法。焚烧炉排出的氮氧化物通过洗涤器或高温装置除去。
2、防护措施
呼吸系统防护:空气中浓度超标时,佩戴过滤式防毒面具(半面罩)。紧急事态抢救或撤离时,建议佩戴氧气呼吸器或空气呼吸器。
眼睛防护:戴化学安全防护眼镜。
身体防护:穿胶布防毒衣。
手防护:戴橡胶手套。
其它:工作现场严禁吸烟、进食和饮水。工作毕,淋浴更衣。
3、急救措施
皮肤接触:立即脱去被污染的衣着,用大量流动清水冲洗,至少15分钟。就医。
眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15分钟。就医。
吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。
食入:误服者用水漱口,给饮牛奶或蛋清。就医。
灭火方法:切断气源。若不能立即切断气源,则不允许熄灭正在燃烧的气体。喷水冷却容器,可能的话将容器从火场移至空旷处。灭火剂:雾状水、抗溶性泡沫、干粉、二氧化碳。
1、本站所有文本、信息、视频文件等,仅代表本站观点或作者本人观点,请网友谨慎参考使用。
2、本站信息均为作者提供和网友推荐收集整理而来,仅供学习和研究使用。
3、对任何由于使用本站内容而引起的诉讼、纠纷,本站不承担任何责任。
4、如有侵犯你版权的,请来信(邮箱:baike52199@gmail.com)指出,核实后,本站将立即删除。













